Vaccino COVID-19 di Sanofi e GSK, dalla fase II conferme di forte risposta immunitaria. Si passa alla fase III
 Il candidato vaccino COVID-19 ricombinante adiuvato di Sanofi e GSK ha raggiunto forti tassi di risposte anticorpali neutralizzanti, in linea con quelle misurate nelle persone che si sono riprese da COVID-19, in tutti i gruppi di età adulta in uno studio di fase 2 con 722 volontari.
Il candidato vaccino COVID-19 ricombinante adiuvato di Sanofi e GSK ha raggiunto forti tassi di risposte anticorpali neutralizzanti, in linea con quelle misurate nelle persone che si sono riprese da COVID-19, in tutti i gruppi di età adulta in uno studio di fase 2 con 722 volontari.
Si prevede che nelle prossime settimane inizierà uno studio globale di Fase 3 che se darà i risultati attesi, dopo le necessarie e delle revisioni normative, dovrebbe essere approvato nel quarto trimestre del 2021.
Il candidato vaccino COVID-19 ricombinante adiuvato di Sanofi e GSK ha raggiunto forti tassi di risposte anticorpali neutralizzanti, in linea con quelle misurate nelle persone che si sono riprese da COVID-19, in tutti i gruppi di età adulta in uno studio di fase 2 con 722 volontari.
I risultati intermedi di Fase 2 hanno mostrato una sieroconversione dal 95% al 100% dopo una seconda iniezione in tutti i gruppi di età (da 18 a 95 anni) e in tutte le dosi, con tollerabilità accettabile e senza problemi di sicurezza. Nel complesso, il candidato al vaccino ha suscitato forti livelli di anticorpi neutralizzanti che erano paragonabili a quelli generati dall’infezione naturale, con livelli più elevati osservati negli adulti più giovani (dai 18 ai 59 anni). Dopo una singola iniezione, sono stati generati alti livelli di anticorpi neutralizzanti nei partecipanti con evidenza di una precedente infezione da SARS-CoV-2, suggerendo un forte potenziale di sviluppo come vaccino di richiamo.
 “I nostri dati di Fase 2 confermano il potenziale di questo vaccino di svolgere un ruolo nell’affrontare questa crisi di salute pubblica globale in corso, poiché sappiamo che saranno necessari più vaccini, soprattutto perché le varianti continuano ad emergere e la necessità di vaccini efficaci e di richiamo, che possono essere conservati a temperature aumentate normali, aumenta” ha affermato Thomas Triomphe, Vicepresidente esecutivo e Capo di Sanofi Pasteur. “Con questi risultati favorevoli, siamo pronti per passare a uno studio globale sull’efficacia di Fase 3. Non vediamo l’ora di generare dati aggiuntivi e di lavorare con i nostri partner in tutto il mondo per rendere disponibile il nostro vaccino il più rapidamente possibile “.
“I nostri dati di Fase 2 confermano il potenziale di questo vaccino di svolgere un ruolo nell’affrontare questa crisi di salute pubblica globale in corso, poiché sappiamo che saranno necessari più vaccini, soprattutto perché le varianti continuano ad emergere e la necessità di vaccini efficaci e di richiamo, che possono essere conservati a temperature aumentate normali, aumenta” ha affermato Thomas Triomphe, Vicepresidente esecutivo e Capo di Sanofi Pasteur. “Con questi risultati favorevoli, siamo pronti per passare a uno studio globale sull’efficacia di Fase 3. Non vediamo l’ora di generare dati aggiuntivi e di lavorare con i nostri partner in tutto il mondo per rendere disponibile il nostro vaccino il più rapidamente possibile “.
Roger Connor, presidente di GSK Vaccines ha aggiunto: “Questi dati positivi mostrano il potenziale di questo candidato vaccino adiuvato a base di proteine nel contesto più ampio della pandemia, inclusa la necessità di affrontare le varianti e di prevedere dosi di richiamo. Riteniamo che questo candidato vaccino possa dare un contributo significativo alla lotta in corso contro COVID-19 e passerà alla Fase 3 il prima possibile per raggiungere il nostro obiettivo di renderlo disponibile entro la fine dell’anno “.
Sulla base di questi risultati intermedi positivi di Fase 2, le aziende prevedono di avviare uno studio globale di fase 3 randomizzato, in doppio cieco con la dose di 10 µg, in combinazione con l’adiuvante pandemico di GSK, nelle prossime settimane. Si prevede che lo studio di fase 3 arruolerà più di 35.000 partecipanti adulti provenienti da un’ampia gamma di paesi e valuterà l’efficacia di due formulazioni di vaccini, comprese le varianti D614 (Wuhan) e B.1.351 (sudafricana).
___________________________________
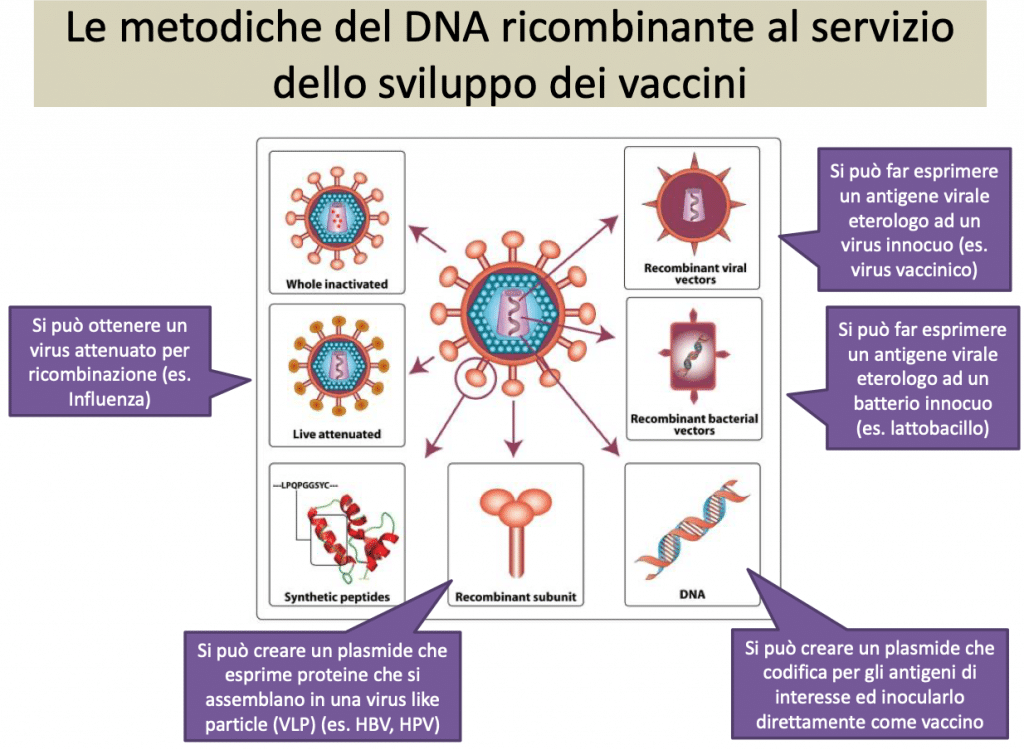 Nota: Il vaccino candidato, sviluppato in collaborazione da Sanofi e GSK, è un vaccino a DNA-ricombinante in subunità basato su una tecnologia consolidata ed è la stessa che Sanofi adotta già con successo per la produzione del vaccino antinfluenzale quadrivalente ricombinante. Proprio l’adozione di questa tecnologia consentirà di produrre un numero notevolmente maggiore di dosi. Lo studio clinico di fase 1/2 è uno studio randomizzato. (fonte Sanofi). GSK fornisce l’adiuvante.
Nota: Il vaccino candidato, sviluppato in collaborazione da Sanofi e GSK, è un vaccino a DNA-ricombinante in subunità basato su una tecnologia consolidata ed è la stessa che Sanofi adotta già con successo per la produzione del vaccino antinfluenzale quadrivalente ricombinante. Proprio l’adozione di questa tecnologia consentirà di produrre un numero notevolmente maggiore di dosi. Lo studio clinico di fase 1/2 è uno studio randomizzato. (fonte Sanofi). GSK fornisce l’adiuvante.
In breve, vaccinare con il DNA consiste nel trasmettere alle cellule dell’ospite i geni che contengono le informazioni necessarie alla cellula per produrre antigeni della proteina “spike” del SARS-CoV-2, la proteina che provocherà una risposta immunitaria specifica con anticorpi diretti contro la stessa proteina “spike”.
I geni vengono inseriti in laboratorio in un virus innocuo per l’uomo (il cosiddetto vettore) che, una volta iniettato, porta i geni fino alla cellula. Qui i geni così iniettati si comportano come qualunque altro gene: vengono copiati in molecole di RNA messaggero (mRNA) che raggiungono i ribosomi – le microscopiche fabbriche di proteine della cellula – e fanno loro produrre la proteina “spike”.
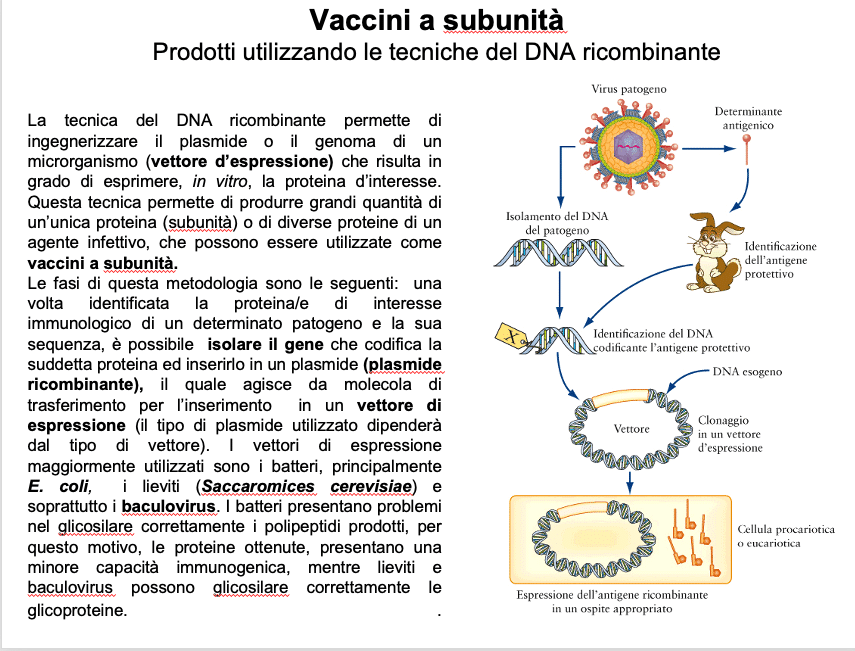 Il DNA ricombinante è utilizzato per produrre OGM in grado, ad esempio, di funzionare come bioreattori per la produzione di ormoni ad uso medico, come l’insulina, l’ormone della crescita o l’ossitocina, o di vaccini. Il bioreattore più utilizzato, anche perché il più facile da trattare, è Escherichia coli, un batterio procariote nel quale può essere inserito un gene da tradurre abbondantemente in proteina (come avviene per i casi appena riportati). Data la scarsa immunogenicità dei vaccini a peptidi e la scarsa efficacia dei vaccini a sub-unità di indurre una risposta cellulo-mediata si sono sviluppate nuove tecnologie adiuvanti per il potenziamento dei vaccini da peptidi o subunità.
Il DNA ricombinante è utilizzato per produrre OGM in grado, ad esempio, di funzionare come bioreattori per la produzione di ormoni ad uso medico, come l’insulina, l’ormone della crescita o l’ossitocina, o di vaccini. Il bioreattore più utilizzato, anche perché il più facile da trattare, è Escherichia coli, un batterio procariote nel quale può essere inserito un gene da tradurre abbondantemente in proteina (come avviene per i casi appena riportati). Data la scarsa immunogenicità dei vaccini a peptidi e la scarsa efficacia dei vaccini a sub-unità di indurre una risposta cellulo-mediata si sono sviluppate nuove tecnologie adiuvanti per il potenziamento dei vaccini da peptidi o subunità.
Sanofi sta anche co-sviluppando un vaccino mRNA per COVID-19 con Translate Bio, che è al passo per iniziare i test sugli esseri umani questo trimestre. Nel frattempo, GSK e Vir Biotechnology hanno lanciato studi di fase III l’anno scorso per VIR-7831, una terapia con anticorpi monoclonali per pazienti adulti ricoverati per COVID-19.
Notizie correlate: Ministero della Salute. Vaccini anti-Covid 19