La Russia di Vladimir Putin ha registrato questa mattina [n.d.r: 11 agosto per chi legge] il primo vaccino anticovid al mondo chiamato “Sputnik  V”. “So che funziona in modo abbastanza efficace, crea un’immunità stabile e, ripeto, ha superato tutti i controlli necessari – dichiara alla Tass il presidente della Federazione – spero che saremo in grado di iniziare prestissimo una produzione di massa, è necessario che tutti possano accedere al vaccino, non sarà un obbligo, ma si accederà su base volontaria
V”. “So che funziona in modo abbastanza efficace, crea un’immunità stabile e, ripeto, ha superato tutti i controlli necessari – dichiara alla Tass il presidente della Federazione – spero che saremo in grado di iniziare prestissimo una produzione di massa, è necessario che tutti possano accedere al vaccino, non sarà un obbligo, ma si accederà su base volontaria
Putin ha rivelato che alla figlia è già stato somministrato il vaccino, che le ha procurato una leggera febbre, sparita poco tempo dopo.
Il vaccino è stato sviluppato congiuntamente dall’Istituto di ricerca Gamaleya e dal Ministero della Difesa della Federazione Russa. I test clinici sul primo vaccino russo per il coronavirus sono iniziati il 18 giugno e hanno visti impegnati 38 volontari, che hanno sviluppato immunità al virus, venendo dimessi il 15 e il 20 luglio scorsi. (fonte Faro di Roma).
Kirill Dmitriev, amministratore delegato del Russian Direct Investment Fund, fondo sovrano della Federazione Russa da 50 miliardi di dollari in gestione, scrive sul sito dedicato www.sputnikvaccine.com:
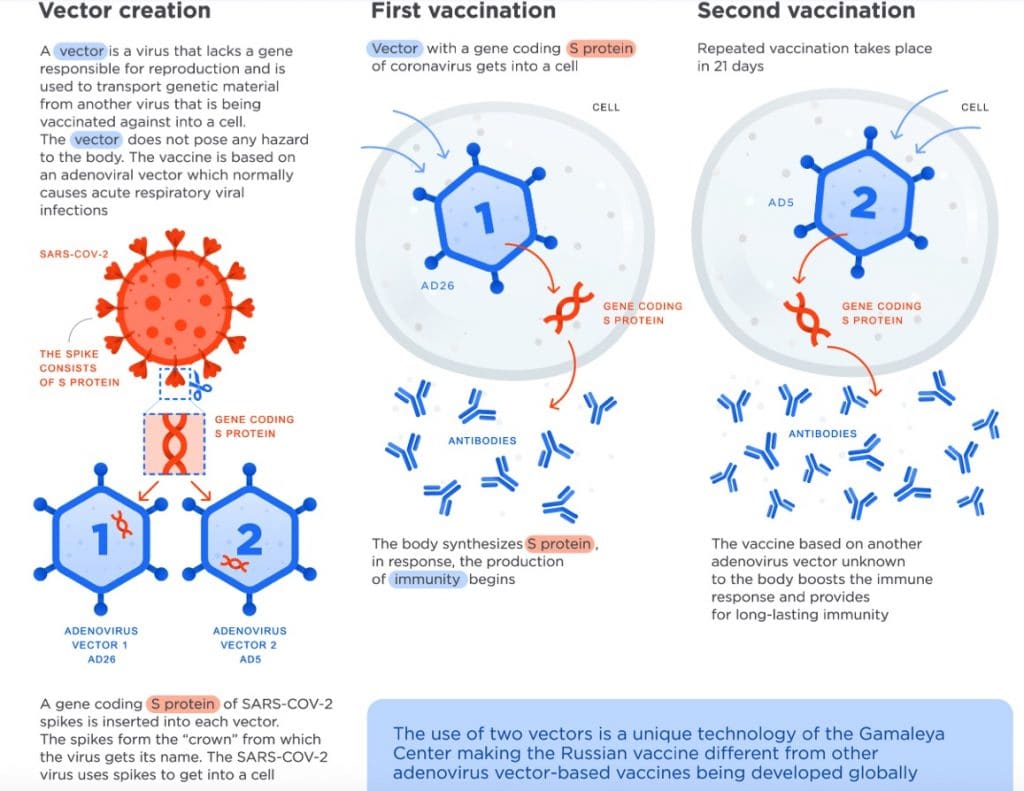
Il Centro Gamaleya ha utilizzato vettori adenovirali per sviluppare vaccini contro l’influenza e contro la sindrome  respiratoria mediorientale (MERS). Entrambi i vaccini sono attualmente in fase avanzata di sperimentazione clinica. Questi risultati mostrano che i laboratori russi non hanno perso tempo negli ultimi decenni, mentre l’industria farmaceutica internazionale ha spesso sottovalutato l’importanza della ricerca sui nuovi vaccini in assenza di minacce per la salute globale prima della pandemia COVID-19.
respiratoria mediorientale (MERS). Entrambi i vaccini sono attualmente in fase avanzata di sperimentazione clinica. Questi risultati mostrano che i laboratori russi non hanno perso tempo negli ultimi decenni, mentre l’industria farmaceutica internazionale ha spesso sottovalutato l’importanza della ricerca sui nuovi vaccini in assenza di minacce per la salute globale prima della pandemia COVID-19.
Altri paesi seguono le nostre orme sviluppando vaccini basati su vettori adenovirali. L’Università di Oxford sta utilizzando l’adenovirus di una scimmia, che non è mai stato utilizzato in un vaccino approvato prima, a differenza degli adenovirus umani. La società statunitense Johnson & Johnson sta utilizzando l’adenovirus Ad26 e la cinese CanSino – l’adenovirus Ad5, gli stessi vettori che utilizza il Gamaleya Center, ma devono ancora padroneggiare l’approccio a due vettori. Entrambe le società hanno già ricevuto ingenti ordini di vaccini dai rispettivi governi.
L’uso di due vettori è la tecnologia unica, sviluppata dagli scienziati del Centro Gamaleya, che differenzia il vaccino russo dagli altri vaccini basati su vettori adenovirali in fase di sviluppo in tutto il mondo. I vaccini basati su vettori adenovirali hanno anche chiari vantaggi rispetto ad altre tecnologie come i vaccini a mRNA (RNA messaggero).
I potenziali vaccini a mRNA, in fase di sperimentazione clinica negli Stati Uniti e in altri paesi, non utilizzano 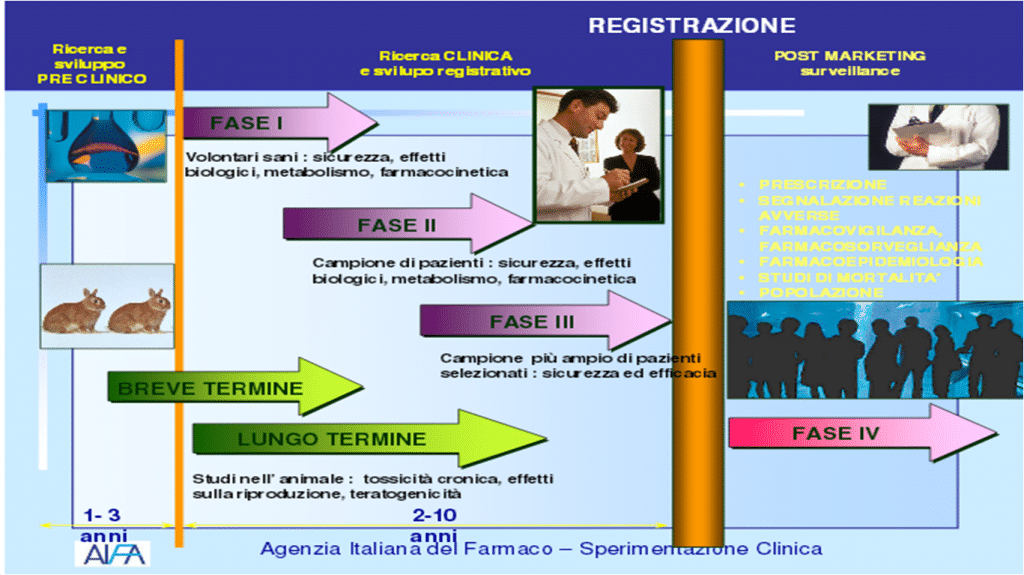 vettori per il rilascio e rappresentano una molecola di RNA con codice proteico del coronavirus avvolto in una membrana lipidica. Questa tecnologia è promettente ma i suoi effetti collaterali, in particolare l’impatto sulla fertilità, non sono ancora stati studiati a fondo. Nessun vaccino a mRNA ha ancora ricevuto l’approvazione normativa nel mondo. Crediamo che nella corsa globale ai vaccini per combattere il coronavirus i vaccini a base di vettori adenovirali saranno i vincitori e che rispetto alla tecnologia mRNA il vaccino Gamaleya sia in vantaggio.
vettori per il rilascio e rappresentano una molecola di RNA con codice proteico del coronavirus avvolto in una membrana lipidica. Questa tecnologia è promettente ma i suoi effetti collaterali, in particolare l’impatto sulla fertilità, non sono ancora stati studiati a fondo. Nessun vaccino a mRNA ha ancora ricevuto l’approvazione normativa nel mondo. Crediamo che nella corsa globale ai vaccini per combattere il coronavirus i vaccini a base di vettori adenovirali saranno i vincitori e che rispetto alla tecnologia mRNA il vaccino Gamaleya sia in vantaggio.
Il vaccino russo è ora pronto e registrato. Le prime due fasi della sperimentazione clinica sono terminate e i loro risultati saranno pubblicati questo mese in linea con i requisiti internazionali. Questi documenti forniranno informazioni dettagliate sul vaccino, inclusi i livelli esatti di anticorpi come mostrato da diversi test di terze parti e  dal test di proprietà di Gamaleya, che identifica gli anticorpi più efficienti che attaccano il picco del coronavirus. Mostreranno anche che tutti i partecipanti agli studi clinici hanno sviluppato un’immunità del 100% al COVID-19. Studi effettuati sui criceti siriani, animali che di solito muoiono a causa del COVID-19, hanno mostrato una protezione del 100% e un’assenza di danni ai polmoni dopo aver ricevuto una dose di infezione letale. Dopo la registrazione condurremo sperimentazioni cliniche internazionali in altri 3 paesi. La produzione di massa dovrebbe iniziare entro settembre e vediamo già un forte interesse globale per il nostro vaccino.
dal test di proprietà di Gamaleya, che identifica gli anticorpi più efficienti che attaccano il picco del coronavirus. Mostreranno anche che tutti i partecipanti agli studi clinici hanno sviluppato un’immunità del 100% al COVID-19. Studi effettuati sui criceti siriani, animali che di solito muoiono a causa del COVID-19, hanno mostrato una protezione del 100% e un’assenza di danni ai polmoni dopo aver ricevuto una dose di infezione letale. Dopo la registrazione condurremo sperimentazioni cliniche internazionali in altri 3 paesi. La produzione di massa dovrebbe iniziare entro settembre e vediamo già un forte interesse globale per il nostro vaccino.
Lo scetticismo tra i media internazionali e i politici è emerso proprio quando la Russia ha annunciato i suoi piani per la produzione di massa del vaccino COVID-19. Quando ho parlato con i media occidentali, molti si sono rifiutati di includere i fatti chiave sulla ricerca russa sul vaccino COVID-19 nelle loro narrazioni. Consideriamo questo scetticismo come un tentativo di minare i nostri sforzi per sviluppare un vaccino efficace, che fermerà la pandemia e aiuterà a riattivare l’economia globale.
Mosca non ha però reso disponibili le evidenze scientifiche sul farmaco, dunque gli esperti non sono in grado di confermarne né la sicurezza né l’efficacia dichiarata dal Cremlino. Un punto su cui interviene l’Organizzazione mondiale della Sanità che, pur dichiarando di essere “in stretto contatto con le autorità sanitarie russe e sono in corso discussioni in merito alla possibile prequalificazione del vaccino da parte dell’Oms”, puntualizza che “la prequalificazione di qualsiasi vaccino include la rigorosa revisione e valutazione di tutti i dati di sicurezza ed efficacia richiesti”.
Stoccata al Cremlino anche da parte dell’Associazione delle organizzazioni per i trial clinici della Russia secondo cui “l’approvazione accelerata non renderà la Russia leader nella corsa” ai vaccini contro il Covid-19, ma “esporrà soltanto i consumatori del vaccino a un pericolo non necessario”. L’associazione ha dunque chiesto al governo di rinviare il via all’uso del vaccino fino a quando non saranno stati condotti e conclusi trial di tipo avanzato che saranno avviati mercoledì. E anche per il ministro della sanità americano, Alex Azar, “il punto è avere un vaccino sicuro per gli americani e per il mondo, non essere i primi”.
 Negli Usa intanto c’è “cauto ottimismo” per lo sviluppo del vaccino realizzato da Moderna Inc e dal National Institute of Allergy and Infectious Diseases. Perplessità anche del governo tedesco che esprime dubbi sulla “qualità, l’efficacia e l’assenza di rischio” del vaccino russo. “L’autorizzazione di un vaccino in Europa richiede sufficienti conoscenze di test clinici per provare l’efficacia e l’assenza di rischio oltre alla prova della qualità farmaceutica” ha detto una portavoce del dicastero della Salute.
Negli Usa intanto c’è “cauto ottimismo” per lo sviluppo del vaccino realizzato da Moderna Inc e dal National Institute of Allergy and Infectious Diseases. Perplessità anche del governo tedesco che esprime dubbi sulla “qualità, l’efficacia e l’assenza di rischio” del vaccino russo. “L’autorizzazione di un vaccino in Europa richiede sufficienti conoscenze di test clinici per provare l’efficacia e l’assenza di rischio oltre alla prova della qualità farmaceutica” ha detto una portavoce del dicastero della Salute.
Anche Massimo Galli, infettivologo dell’ospedale Sacco di Milano, esprime perplessità: “Finché non avremo dati confermati si tratta solo di un annuncio giornalistico. Sarebbe bellissimo se fosse vero, ma devo esprimere delle riserve fino a quando non avremo evidenze”. “Sarebbe una notizia fantastica – dice Galli all’Adnkronos Salute – ma è difficile visto che le modalità e le caratteristiche per l’approntamento di un vaccino sono diverse da queste, a meno che non siano stati resi noti tutti i dati necessari precedenti, sulla sicurezza e l’efficacia, di cui non ho notizia”. “Per arrivare a questo risultato – precisa Galli – si passa per una serie di fasi, almeno nei Paesi in cui si rispettano i trattati internazionali sulla sperimentazione, validazione e valutazione della tossicità potenziale di farmaci e vaccini”. (fonte Il Fatto Quotidiano).
“Non funziona così: non si può saltare la fase III di un vaccino, dopo aver fatto 2 piccoli studi su 76 volontari, di cui nessuno sa nulla, e poi proclamare che siccome il vaccino ha funzionato su una figlia, ormai è pronto. Senza dati solidi, in queste condizioni non mi vaccinerei nemmeno io. Per fortuna, i vaccini” per il coronavirus Sars-Cov-2 “in sviluppo sono circa 200, e dei 4 più avanzati sappiamo molto, molto di più”. E’ la riflessione che Enrico Bucci, ricercatore in Biochimica e Biologia molecolare e professore alla Temple University di Filadelfia
Notizie correlate:
Sputnik V clinical trials
Binnopharm, l’azienda russa che produrrà il vaccino anti Covid (di Putin)
Nature. Russia’s fast-track coronavirus vaccine draws outrage over safety
AIFA. La sperimentazione clinica dei farmaci
AIFA.
Le fasi di sviluppo di un vaccino
Lo sviluppo di un vaccino è un processo piuttosto lungo ed elaborato che parte dalla conoscenza del microrganismo responsabile della malattia che si intende prevenire e delle sue modalità di interazione con l’organismo umano. Inizialmente si effettuano studi sperimentali in vitro, in base ai quali è possibile stabilire quale sia la composizione qualitativa e quantitativa ideale di un vaccino (tipologia e quantità della componente attiva e di tutte le altre sostanze previste).
Una volta definito questo aspetto, il potenziale vaccino viene sottoposto alla sperimentazione pre-clinica che include studi in vitro e su modelli animali attraverso i quali si definiscono il meccanismo d’azione (cioè la capacità di indurre la risposta immunitaria), il profilo tossicologico e le prime evidenze di efficacia e sicurezza su un organismo vivente complesso.
Questa fase permette di selezionare la formulazione che nei modelli sperimentali è risultata più promettente per essere avviata alla fase clinica preliminare sull’uomo. Per i vaccini multicomponente è necessario che in questa fase venga studiata inoltre la possibile interferenza fra le varie componenti attive del vaccino.
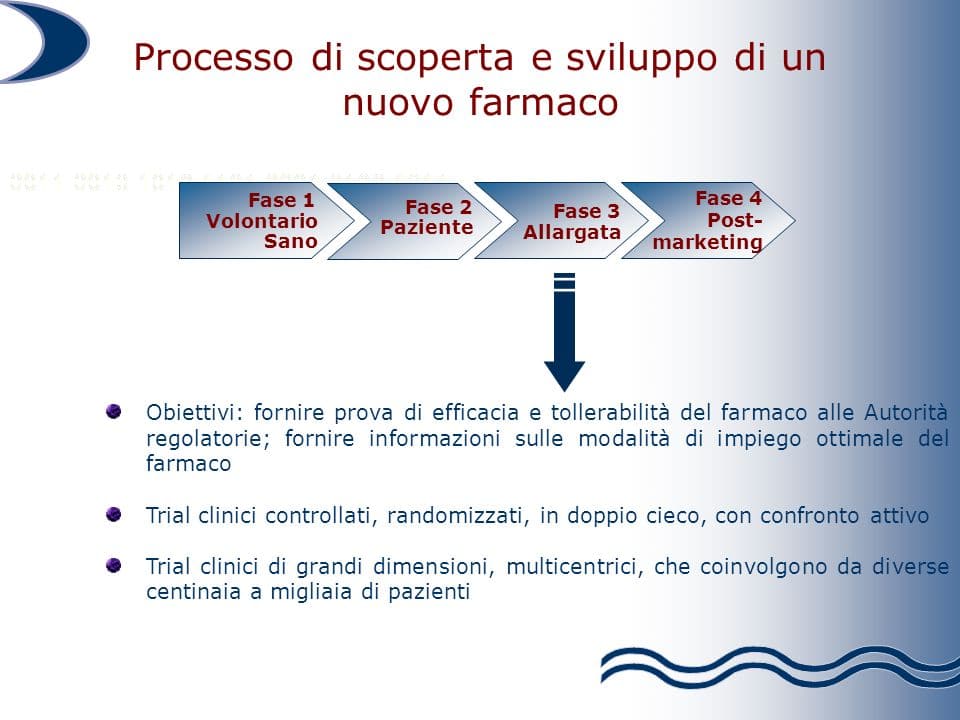
A questo punto, il vaccino entra nel percorso di sperimentazione clinica che può realizzarsi in quattro fasi: le prime tre precedono l’autorizzazione all’immissione in commercio e la quarta viene condotta quando il vaccino è già disponibile sul mercato.
Durante le prime tre fasi, viene progressivamente aumentata la popolazione trattata con il vaccino, definita la posologia (numero di dosi per l’immunizzazione primaria ed eventuale richiamo) e caratterizzata l’efficacia del vaccino o immunogenicità (la capacità di stimolare nell’uomo una risposta anticorpale specifica e sufficiente contro le componenti del vaccino) e la sicurezza o reattogenicità (il tipo e la frequenza con cui si manifestano eventuali reazioni avverse). Questi ultimi due aspetti vengono indagati soprattutto negli studi clinici di fase terza, condotti su popolazioni molto ampie di soggetti a cui sarà destinato il vaccino.
In questi studi vengono infatti confermate l’efficacia (in termini di tipologia e persistenza della risposta immunitaria, percentuale dei soggetti che rispondono efficacemente al vaccino e, quando possibile, di riduzione della probabilità di sviluppare la malattia dopo la vaccinazione) e la sicurezza del vaccino (in termini di eventi avversi attribuibili e non attribuibili al vaccino e di possibili problemi legati alle caratteristiche dei soggetti come l’età, il sesso e specifiche condizioni di salute).
In queste tre fasi, inoltre, viene esplorata la possibilità di somministrare il vaccino in sviluppo insieme ad altri vaccini già in commercio in particolari categorie di soggetti per ottenere informazioni specifiche sulle possibili interferenze in termini di efficacia e sicurezza.
Gli studi di fase terza sono:
- controllati, dal momento che i soggetti trattati con il vaccino in studio sono confrontati con altrettanti soggetti trattati con un vaccino simile già autorizzato o con un trattamento inerte (placebo)
- randomizzati, dal momento che la suddivisione dei soggetti fra l’uno e l’altro trattamento avviene in maniera casuale
Questa tipologia di studi rappresenta lo strumento più solido del metodo scientifico per dimostrare l’efficacia e la sicurezza di un prodotto medicinale, inclusi i vaccini, in quanto permette di attribuire con ragionevole certezza le differenze osservate nei soggetti coinvolti nello studio esclusivamente al medicinale/vaccino.
Gli studi di fase quarta (o studi post-autorizzativi) vengono condotti dopo la commercializzazione e hanno l’obiettivo di verificare l’efficacia e la sicurezza del vaccino nelle sue reali condizioni d’uso, di valutarne l’utilizzo in particolari sottogruppi di popolazioni e condizioni patologiche (per esempio in corso di malattie del sistema immunitario che potrebbero modificare l’efficacia e la sicurezza del vaccino) e il rapporto costo-beneficio rispetto alla malattia e/o ad altri vaccini.
Tutte le varie fasi dello sviluppo di un vaccino sono necessarie a ottenere informazioni il più possibile chiare ed esaustive su indicazioni, controindicazioni, avvertenze speciali, benefici e rischi del prodotto. Poiché i vaccini vengono somministrati a scopo preventivo in una popolazione sana, è necessario che le percentuali di efficacia siano molto alte (numero di soggetti che rispondono in maniera adeguata al vaccino) e che il beneficio sia di gran lunga superiore al rischio.
Pertanto, in ogni momento di tutto questo processo, lo sviluppo del vaccino o la sua commercializzazione possono essere interrotti, qualora venga meno una sola di queste condizioni fondamentali.
Tutti gli studi effettuati durante lo sviluppo di un vaccino (come per tutti i medicinali) devono rispondere agli standard internazionali di etica e qualità scientifica previsti dalle norme di buona pratica clinica, codificate a livello globale (Good Clinical Practice, GCP).