Brexit, la filiera del farmaco è preoccupata. Rischio per carenze e mobilità professionale
Federfarma – 15 febbraoio 2019
L’ipotesi di una Brexit “hard”, un no-deal che inchiodi gli scambi tra Regno Unito ed Unione europea dopo il 29 marzo, inizia ad entrare nel campo delle probabilità e a preoccupare non poco tutta la filiera del farmaco. Tanto che qualche azienda ha già pensato di attrezzarsi al peggio. Il settore più coinvolto, infatti, al momento pare quello farmaceutico, dove già da tempo le autorità britanniche sono intervenute chiedendo ai produttori di incrementare le scorte. Richiesta ribadita anche il 17 gennaio scorso in  una lettera spedita dal dipartimento della Salute e dell’Assistenza Sociale alla Federazione europea di settore e circolata poi tra numerose aziende.
una lettera spedita dal dipartimento della Salute e dell’Assistenza Sociale alla Federazione europea di settore e circolata poi tra numerose aziende.
Anche il Pharmaceutical Group of the European Union (Pgeu), l’Associazione che rappresenta gli interessi delle farmacie e dei farmacisti territoriali nell’Ue, ha mostrato preoccupazione per questo scenario in considerazione del fatto che ogni mese, 45 milioni di confezioni di medicine sono fornite dal Regno Unito al resto d’Europa. “Il Regno Unito è un attore chiave nel settore farmaceutico europeo – ha spiegato Roberto Tobia, tesoriere di Federfarma e delegato del presidente Marco Cossolo al Pgeu – rappresentando il 10% della produzione totale dell’Ue e contribuendo a circa il 20% del totale degli investimenti in R&S. Questo ci da la dimensione di un problema che se non troverà la giusta dimensione con un accordo entro fine marzo ci porterà a non poche difficoltà per il mercato del farmaco oltre che per la mobilità professionale, ovvero il riconoscimento delle qualifiche professionali, con un blocco per i farmacisti italiani, laureati dopo il 29 marzo p.v., che volessero prestare la propria attività professionale nel Regno Unito”.
Secondo una recente analisi sulla questione Brexit, anche un’uscita ordinata, ovvero un accordo tra le parti, può avere numerose conseguenze: tempi maggiorati per 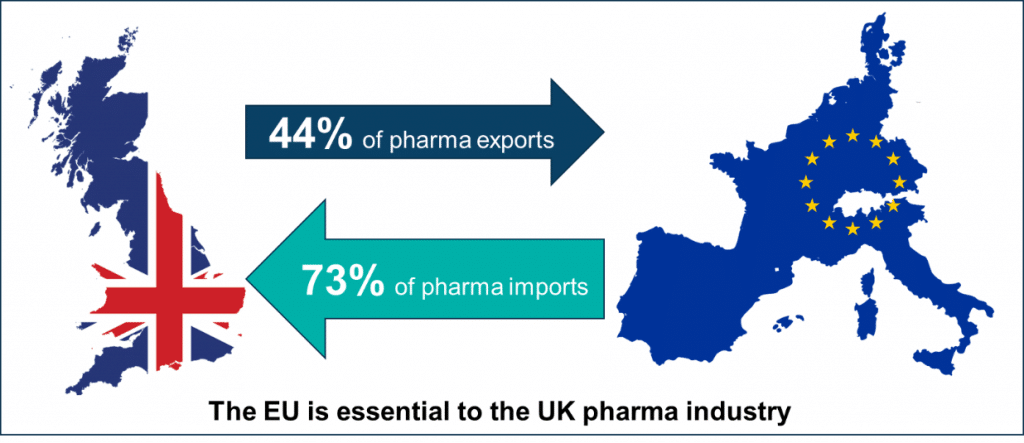 l’autorizzazione alla commercializzazione di farmaci e dispositivi medici a causa delle necessarie duplicazioni degli iter autorizzativi, e, quindi, ritardi nell’accesso ai farmaci per la popolazione. Senza parlare dei ritardi che verrebbero, invece, imposti dal ripristino delle frontiere e quindi tariffe e controlli tecnici che non potranno che ritardare la fornitura di medicinali e dispositivi medici e portare ad un aumento generale dei costi.
l’autorizzazione alla commercializzazione di farmaci e dispositivi medici a causa delle necessarie duplicazioni degli iter autorizzativi, e, quindi, ritardi nell’accesso ai farmaci per la popolazione. Senza parlare dei ritardi che verrebbero, invece, imposti dal ripristino delle frontiere e quindi tariffe e controlli tecnici che non potranno che ritardare la fornitura di medicinali e dispositivi medici e portare ad un aumento generale dei costi.
“Difficoltà e rallentamenti dovuti al fatto che il Regno Unito potrebbe diventare a breve un Paese terzo senza alcun accordo che permetta una transizione ordinata – aggiunge Tobia – potrebbe portare al problema più grande e più temuto: nuove carenze di farmaci essenziali in vari Paesi Europei. L’Ema ha già calcolato a rischio carenze 19 farmaci registrati a Londra, a questi si dovranno aggiungere i farmaci autorizzati con la procedura decentrata, ovvero quelli che hanno ottenuto la registrazione grazie al fatto che le procedure erano state effettuate nel Regno Unito, scelto come Paese di riferimento grazie all’efficienza dell’Aifa locale (la Medicines and Healthcare Products Regulatory Agency). Per questi farmaci il processo autorizzativo dovrebbe ripartire quasi da zero”.