Coronavirus, corsa al vaccino. La casa farmaceutica Moderna: “Il nostro efficace al 94.5%”
Quotidiano italiano – 16 novembre 2020
 Dopo l’annuncio di Pfizer e BioNtech, arriva anche il vaccino della casa farmaceutica americana Moderna, con una efficacia pari al 94.5%, rispetto al 90% del vaccino tedesco.
Dopo l’annuncio di Pfizer e BioNtech, arriva anche il vaccino della casa farmaceutica americana Moderna, con una efficacia pari al 94.5%, rispetto al 90% del vaccino tedesco.
Le prime 20 milioni di dosi saranno destinate al mercato americano e si calcola saranno prodotte entro il 2020. L’anno prossimo invece, le altre dosi comprese tra 500 milioni e un miliardo, saranno destinate al mercato globale.
Il prezzo, stando ad alcune notizie, è di 25 dollari e includerà probabilmente anche una quota di profitto. Le altre aziende finora hanno annunciato che lo venderanno a prezzo di costo, almeno fino a quando permarrà la dichiarazione di pandemia.
Al momento, stando alle notizie apprese, il vaccino di Moderna non ha effetti collaterali se non qualche linea di febbre e indolenzimento nel punto dell’iniezione. Rispetto al vaccino della Pfizer, la seconda dose dovrà essere somministrata dopo quattro settimane.
La fase sperimentale è iniziata il 27 luglio, lo stesso giorno di Pzifer, e ha coinvolto 30mila volontari. A metà è stato somministrato il vaccino, all’altra metà un placebo.
Tra quelli a cui è stato somministrato il placebo, in 90 si sono ammalati, 11 gravemente, mentre quelli sottoposti a vaccino solo in 5 hanno contratto il covid, ma non in forma grave. Quindici dei 95 contagiati avevano più di 65 anni. Da questi numeri si calcola il valore dell’efficacia, che è appunto del 94,5%.
Al momento è lasciata aperta la domanda sul tipo di immunità: se sterilizzante (il vaccino impedisce di infettarsi e di contagiare gli altri) o solo dai sintomi (i vaccinati non si ammalano in modo grave ma possono trasmettere il virus agli altri).
 Nota: L’azienda biotecnologica americana Moderna ha reso noti i dati di fase 3 di sperimentazione sull’uomo per il vaccino mRNA-1273 dal quale risulta un’efficacia che sfiora il 95% (94,5). Inoltre il vaccino può essere conservato a una temperatura compresa tra i 2 e 8 gradi (valori garantiti da un frigorifero domestico) per 30 giorni (rispetto ai 7 stimati in una fase precedente di studio), senza necessità di essere conservato in freezer. La “stabilità” del farmaco è invece di 12 ore a temperatura ambiente.
Nota: L’azienda biotecnologica americana Moderna ha reso noti i dati di fase 3 di sperimentazione sull’uomo per il vaccino mRNA-1273 dal quale risulta un’efficacia che sfiora il 95% (94,5). Inoltre il vaccino può essere conservato a una temperatura compresa tra i 2 e 8 gradi (valori garantiti da un frigorifero domestico) per 30 giorni (rispetto ai 7 stimati in una fase precedente di studio), senza necessità di essere conservato in freezer. La “stabilità” del farmaco è invece di 12 ore a temperatura ambiente.
Lo studio di Moderna, denominato COVE, illustra l’efficacia del vaccino sulla base dei casi confermati di Covid-19 nell’arco di due settimane dalla somministrazione. Su 95 volontari, 90 avevano ricevuto un placebo, solo in cinque di loro era presente l’mRNA-1273. Undici persone appartenenti al gruppo placebo hanno sviluppato forme gravi della malattia, tutti i cinque vaccinati sono risultati invece negativi.
Il limite di questo riscontro, oltre alla evidente preliminarietà – come riportano gli stessi autori – consiste nel fatto che i nuovi casi tendono a palesarsi nel tempo, questo potrebbe portare a un aggiornamento della loro stima. È infatti sulla base di questo singolo riscontro che leggiamo di una efficacia del 94,5%. Del resto sul totale di 95 persone, 15 erano over 65, ovvero i soggetti più a rischio. Non sappiamo al momento come erano distribuiti tra gruppo di controllo (quello a cui è stato somministrato il placebo) e gruppo di persone effettivamente vaccinate.
Del resto, gli autori del comunicato assicurano che «L’analisi preliminare suggerisce un profilo di sicurezza ed efficacia sostanzialmente coerente in tutti i sottogruppi valutati». Così come nel caso di Pfizer, è molto improbabile che si lancino annunci iperbolici in queste ultime fasi, anche se sarebbe meglio attendere di leggere degli studi veri e propri, prima di cantare vittoria.
Le prime dosi del vaccino di Moderna, tutte quelle del 2020, sono riservate agli Stati Uniti. “Per gli impianti di fabbricazione in Svizzera e Spagna abbiamo fatto tutti gli investimenti da soli, senza supporto locale” sottolinea Zaks, Chief medical officer dell’azienda di Cambridge, Massachusetts
Notizie correlate: mRNA-1273, Moderna’s Potential Vaccine Against COVID-19 (video)
Moderna Completes Enrollment of Phase 3 COVE Study of mRNA Vaccine Against COVID-19 (mRNA-1273)
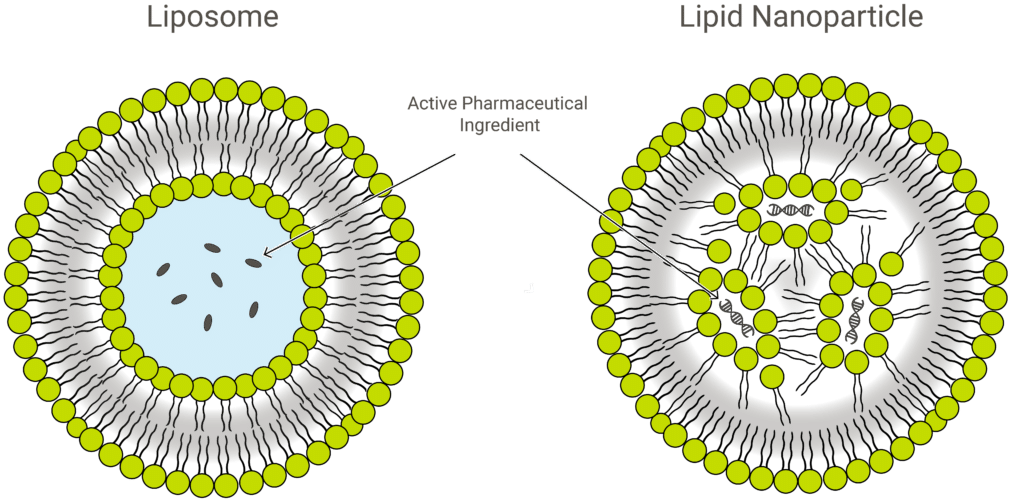
Iniettare una sequenza di mRNA in modo che entri nella cellula non è un passaggio semplice. Difatti, nel nostro corpo sono presenti le ribonucleasi, enzimi che catalizzano l’idrolisi dell’RNA e rendono quindi rischioso il viaggio del ribonucleotide. Inoltre, per l’mRNA carico negativamente è difficile attraversare la membrana plasmatica. La soluzione è un sistema di trasporto che garantisca l’accesso all’mRNA integro nella cellula, senza dover usare un vettore virale: le nanoparticelle lipidiche (LNP). Questa struttura trasporta la molecola di interesse proteggendola con un doppio strato lipidico. Vediamo quali sono i vantaggi che ne conseguono.
- Il vaccino non contiene agenti patogeni attenuati: non è infettivo
- L’mRNA non necessita di entrare nel nucleo in quanto la sintesi proteica avviene nel citoplasma: questo facilita la sua attività
- Il vaccino a mRNA può essere prodotto molto rapidamente, caratteristica fondamentale nel mezzo di una pandemia
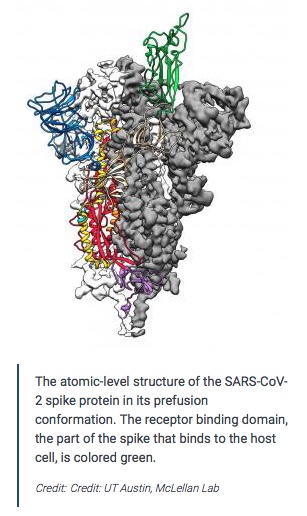
AstraZeneca, Janssen e CanSino Biologics utilizzano invece dei vettori virali (virus resi innocui e incapaci di infettare), per agevolare il trasporto di un frammento di RNA codificante l’antigene o la sequenza RNA del virus (in laboratorio), che sintetizzano proteine o frammenti di proteine del capside virale. Conseguentemente, iniettandole nell’organismo combinate con sostanze che esaltano la risposta immunitaria, si induce la risposta anticorpale da parte dell’individuo. Il vaccino russo Gam-COVID-Vac (Sputnik V) è un vaccino a due vettori basato sull’adenovirus umano che esprime la proteina spike di SARS-CoV-2 per stimolare una risposta immunitaria.
Il vaccino basato sull’adenovirus Ad26 viene utilizzato per la prima dose e il vaccino basato sull’adenovirus Ad5 viene utilizzato il 21° giorno per potenziare la risposta immunitaria.
Nuovo coronavirus: il punto sui vaccini in sperimentazione