In Europa, nel corso del 2022, sono stati autorizzati 89 nuovi medicinali, di cui 48 contenenti nuove sostanze attive, 8 biosimilari, 23 equivalenti e 10 tra medicinali ibridi, sostanze attive note e farmaci autorizzati con la procedura del consenso informato.
Gli antineoplastici e immunomodulatori – destinati al trattamento di alcuni tipi di tumori solidi (quali il tumore del polmone, della prostata e del fegato), del sangue (quali mieloma, linfoma e leucemia) e delle malattie autoimmuni – si confermano le categorie più rappresentate (complessivamente il 37,5%) tra i medicinali contenenti nuovi principi attivi autorizzati dall’Agenzia Europea per i Medicinali (EMA). Seguono, in ordine decrescente, gli antinfettivi ad uso sistemico, i farmaci dell’apparato gastrointestinale e metabolismo, del sistema nervoso.
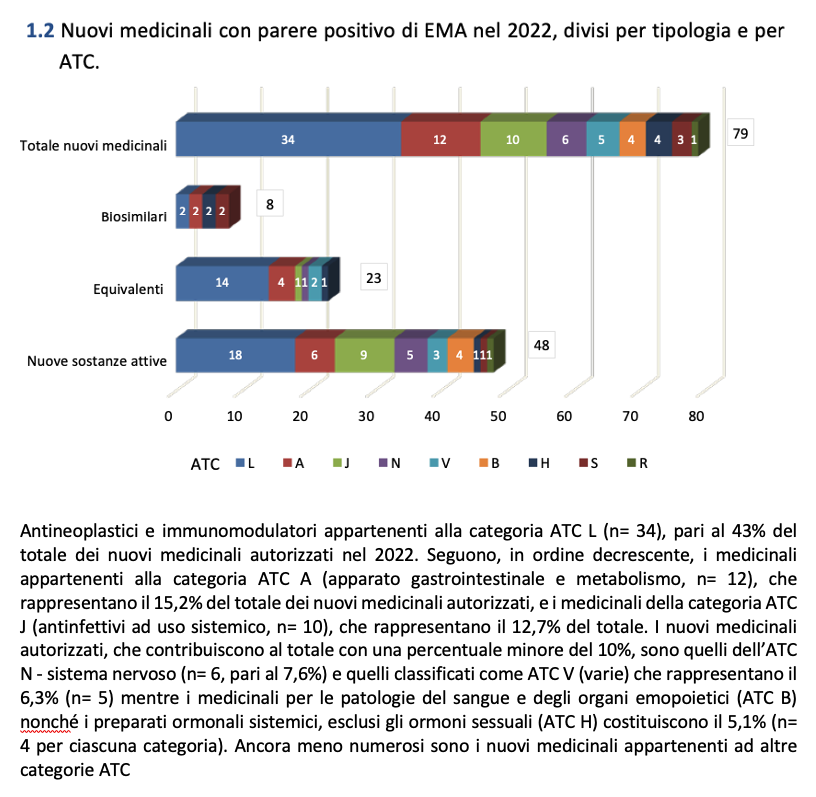 Sono alcune delle informazioni contenute nella 5^ edizione del Rapporto “Horizon Scanning: scenario dei medicinali in arrivo”, pubblicato dall’Agenzia Italiana del Farmaco con lo scopo di fornire informazioni sui nuovi medicinali e sulle nuove terapie, che hanno ricevuto un parere positivo dell’EMA o che potrebbero averlo negli anni successivi. L’analisi, in particolare, si concentra su medicinali contenenti nuove sostanze attive, biosimilari ed equivalenti, per un totale di 79 nuovi medicinali autorizzati.
Sono alcune delle informazioni contenute nella 5^ edizione del Rapporto “Horizon Scanning: scenario dei medicinali in arrivo”, pubblicato dall’Agenzia Italiana del Farmaco con lo scopo di fornire informazioni sui nuovi medicinali e sulle nuove terapie, che hanno ricevuto un parere positivo dell’EMA o che potrebbero averlo negli anni successivi. L’analisi, in particolare, si concentra su medicinali contenenti nuove sostanze attive, biosimilari ed equivalenti, per un totale di 79 nuovi medicinali autorizzati.
Nel corso del 2022 EMA ha autorizzato 20 medicinali orfani contenenti nuove sostanze attive, 5 dei quali sono medicinali per terapie avanzate (nello specifico, terapie geniche), e espresso parere positivo su 91 nuove indicazioni di 67 medicinali già autorizzati. Il maggior numero di nuove indicazioni terapeutiche riguarda i farmaci antineoplastici e immunomodulatori, che con 43 nuove indicazioni rappresentano il 47,3% del totale.
Novantadue sono invece i nuovi medicinali in valutazione presso l’EMA all’inizio del 2023, con parere atteso nel corso dell’anno: 61 sono farmaci contenenti nuove sostanze attive (di cui 28 sono medicinali orfani), 17 sono equivalenti e 14 sono biosimilari. I più numerosi sono gli antineoplastici (25), seguiti dagli immunosoppressori (14) e dai medicinali del sistema nervoso (6).
Sono in valutazione anche 64 nuove indicazioni terapeutiche (per un totale di 58 medicinali già autorizzati), appartenenti a 9 aree principali: tumori solidi, malattie infettive, malattie autoimmuni e allergie, tumori del sangue, malattie neurologiche, neurometaboliche e sensoriali, cardiovascolari e sindromi metaboliche.
Infine sono 111 i medicinali ammessi al programma PRIME, rivolto ai farmaci promettenti e ad elevato interesse per la salute pubblica, destinati a pazienti con esigenze di cura insoddisfatte, per i quali è previsto supporto precoce allo sviluppo. Si tratta, per la maggior parte, di terapie avanzate e l’area oncologica è la più rappresentata, seguita dalle aree di ematologia-emostasiologia, endocrinologia-ginecologia-metabolismo, neurologia e dai vaccini.
AIFA – Pubblicato il: 04 aprile 2023
AIFA – Horizon Scanning. Rapporto Anno 2023. Roma: Agenzia Italiana del Farmaco, 2023